
Kandungan
Bahagian lainHidrogen adalah unsur paling ringan dan mempunyai banyak kegunaan industri, termasuk penciptaan lemak terhidrogenasi untuk digunakan di dapur dan pengeluaran hidrokarbon dari arang batu. Ini adalah bahagian penting molekul air dan dapat dipisahkan dengan menggunakan sebilangan kecil elektrik. Anda juga boleh menghasilkan gas hidrogen menggunakan beberapa logam aktif dan asid kuat. Kedua-dua kaedah ini agak mudah dan akan membolehkan anda mengumpulkan gas hidrogen.
Langkah-langkah
Kaedah 1 dari 2: Menggunakan Pemindahan Air dengan Logam Aktif
Kumpulkan bahan yang diperlukan. Untuk mengumpulkan hidrogen menggunakan reaksi mencampurkan asid kuat dengan logam aktif, anda memerlukan: labu Erlenmeyer, penyumbat getah, tiub plastik, air suling, tabung uji, bekas besar, asid hidroklorik 3 molar (HCl), dan pelet magnesium atau zink.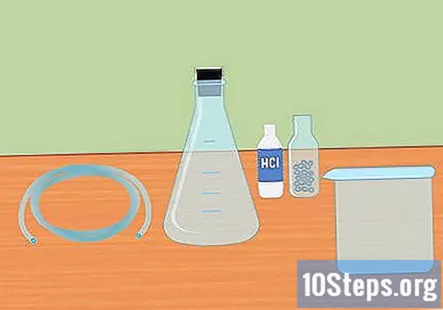
- Kelalang Erlenmeyer adalah termos kaca yang mempunyai bahagian bawah kerucut dan leher silinder.
- Penyumbat getah adalah untuk bahagian atas termos dan perlu mempunyai lubang di bahagian tengah agar saluran paip dapat dilalui.
- Sama ada magnesium atau zink akan berfungsi untuk percubaan ini, anda tidak memerlukan kedua-duanya.
- Sebilangan bekalan ini mungkin perlu dibeli secara dalam talian atau di kedai bekalan makmal.

Pakai alat pelindung yang betul. Semasa bekerja dengan asid kuat seperti asid hidroklorik, anda ingin memastikan anda mengambil langkah keselamatan yang betul. Memakai kot makmal, sarung tangan, kasut kaki tertutup, dan pelindung mata sangat penting.- Gogal harus membungkus sisi mata anda untuk melindunginya dari percikan.
- Pakai sarung tangan yang sesuai dengan betul sehingga anda dapat menjaga ketangkasan tangan dan jari anda dengan baik.
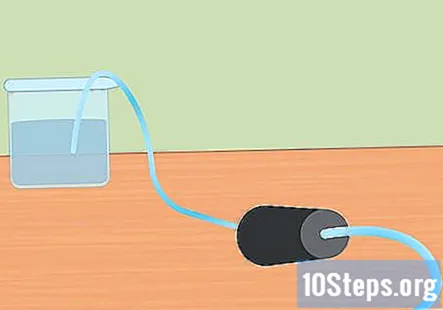
Siapkan persediaan eksperimen. Masukkan satu hujung tiub ke dalam lubang penyumbat getah. Anda mahu tabung berjalan terus melalui penyumbat getah dan keluar sedikit dari hujungnya. Isi bekas besar dengan air dan letakkan hujung tiub bebas ke dalam air. Apabila percubaan bermula, anda akan memasukkan penyumbat getah ke dalam labu Erlenmeyer.- Ketepikan kepingan ini sehingga anda siap menggunakannya.
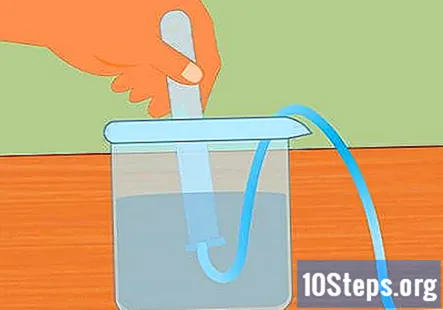
Tenggelam tabung uji di dalam air. Ambil sekurang-kurangnya satu tabung uji (anda boleh menggunakan lebih banyak jika anda ingin mengumpulkan lebih banyak hidrogen) dan masukkan ke dalam air. Condongkan tiub supaya semua gelembung udara dapat keluar. Letakkan tiub di atas tiub terendam yang melekat pada penyumbat getah di hujung yang bertentangan.- Semua gelembung udara dikeluarkan dari tiub sebelum anda memulakannya. Sekiranya tidak, gas yang terkumpul di dalam tiub akan lebih daripada sekadar hidrogen.
Masukkan asid hidroklorik ke dalam termos Erlenmeyer. Masukkan asid hidroklorik secukupnya untuk mengisi termos kira-kira separuh. Lebih kurang 100 mL mesti mencukupi. Pastikan termos bersih dan kering sebelum menambahkan asam. Pakai sarung tangan getah dan berhati-hati semasa mengisi termos.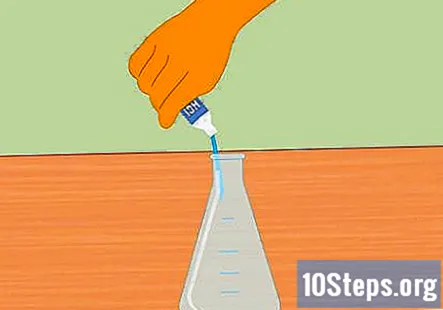
- Berhati-hatilah untuk tidak menumpahkan air ke dalam asid. Air yang ditambahkan ke dalam asid boleh menyebabkan letupan dan kecederaan.
Mulakan tindak balas kimia dengan menambahkan pelet logam ke HCl. Masukkan segelintir pelet zink atau magnesium ke asid hidroklorik dalam termos. Jumlah tepat yang anda masukkan tidak penting, tetapi sebilangan kecil harus cukup untuk memulakan reaksi.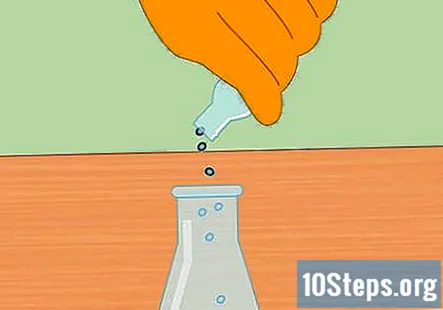
- Setelah menambah pelet, letakkan penyumbat ke dalam labu sehingga sistemnya sekarang ditutup.
Kumpulkan hidrogen dalam tabung uji terendam. Oleh kerana logam bertindak balas dengan asid, gas hidrogen dihasilkan. Hidrogen ini bergerak ke bahagian atas termos, melalui tiub dan ke tabung uji yang terendam di dalam air. Gas akan menggantikan air dan anda akan melihat bentuk gelembung di bahagian atas tabung uji.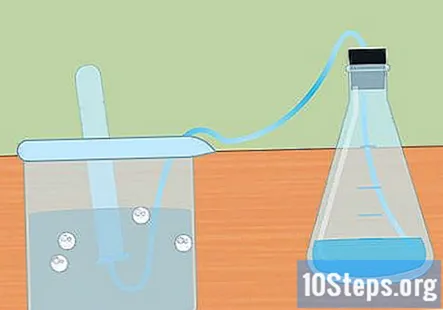
- Apabila tabung uji diisi dengan hidrogen, tenggelamkan tiub lain dengan air dan letakkan di atas tiub. Anda dapat mengumpulkan hidrogen sebanyak yang dihasilkan oleh reaksi anda.
- Pastikan tabung uji menghadap ke bawah untuk mengelakkan gas hidrogen keluar ke udara.
Pastikan gas adalah hidrogen. Untuk mengesahkan bahawa gas itu hidrogen, anda boleh melakukan apa yang disebut ujian splint. Nyalakan sepadan dan tahan di bawah tiub. Anda akan mendengar "pop" atau suara berdecit, yang menunjukkan bahawa hidrogen ada.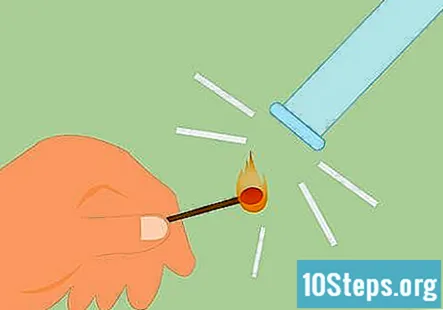
Kaedah 2 dari 2: Menggunakan Elektrolisis
Kumpulkan bahan yang diperlukan. Dalam eksperimen ini, anda akan menggunakan elektrik untuk memisahkan gas hidrogen dan oksigen dari molekul air. Untuk mengumpulkan gas hidrogen menggunakan elektrolisis, anda memerlukan bateri 9 volt, pensil, dua tabung uji, bekas plastik, air, baking soda, dua gelang getah besar (pilihan), dan klip bateri dengan penjepit di hujungnya.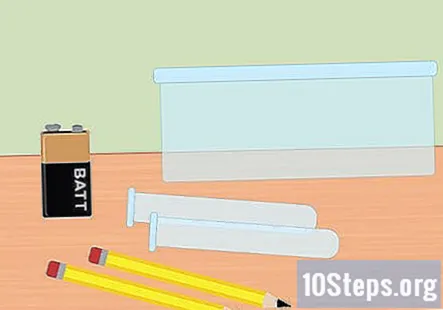
- Pensel mesti mempunyai grafit di dalamnya agar ini berfungsi. Pensel nombor 2 sangat sesuai. Dua kepingan grafit kecil juga akan berfungsi untuk ini.
- Bekas atau mangkuk simpanan makanan kecil sudah mencukupi.
- Pastikan klip bateri boleh memuatkan bateri 9 volt dan ia mempunyai wayar merah dan hitam dengan pengapit buaya di hujungnya. Pengapit ini akan digunakan untuk menghubungkan sistem anda ke bateri.
Keluarkan pemadam dari pensil dan pecahkan pensel menjadi dua. Anda memerlukan dua keping grafit, satu untuk hujung bateri positif dan hujung bateri negatif. Tajamkan kedua-dua hujung pensil ke satu titik. Pastikan grafit terdedah dengan baik.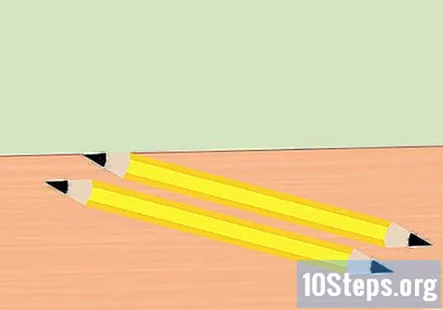
- Langkah ini boleh dilangkau jika anda sudah mempunyai dua keping grafit tulen.
Balut 2 gelang getah di sekitar bekas dalam bentuk X. Langkah ini adalah pilihan, tetapi merupakan kaedah mudah untuk mengekalkan tabung uji semasa eksperimen dijalankan. Regangkan satu jalur getah di atas bekas dan panjangkan jalur getah kedua di atasnya sehingga melintasi yang pertama, membentuk X.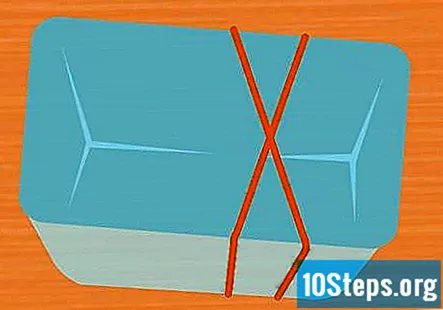
- Sekiranya anda tidak menggunakan gelang getah, pastikan untuk mengikat tabung uji dengan pita atau tali supaya ia terbalik semasa percubaan.
Buat larutan soda penaik dan air. Melarutkan baking soda di dalam air akan membantu elektrik dalam sistem. Jumlah tepat penaik soda tidak penting, tetapi kira-kira 1 sudu teh setiap 1 cawan air harus mencukupi. Kacau hingga larut sepenuhnya.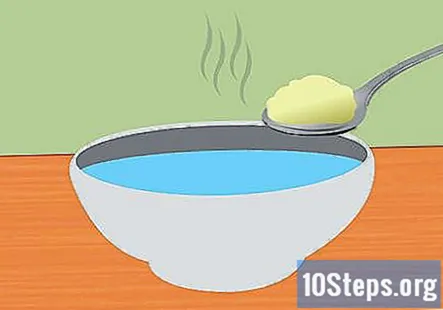
- Gunakan air suam untuk mempercepat larutan soda penaik.
Isi bekas plastik dan tabung uji dengan larutan baking soda. Bekas perlu cukup besar untuk menahan kedua tabung uji. Tambahkan cukup larutan untuk mengisi bekas kira-kira tiga perempat penuh. Rendam tabung uji dalam larutan bekas dan balikkan terbalik. Letakkan setiap tiub di salib gelang getah X untuk menahannya di tempatnya.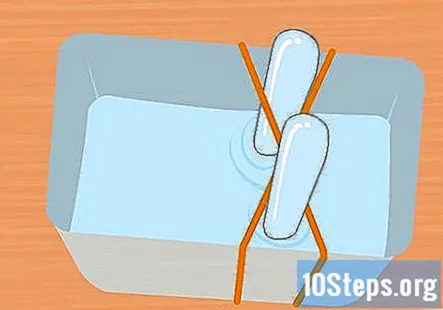
- Adalah sangat penting bahawa kedua-dua tabung uji penuh dengan air dan tidak ada gelembung udara yang tersisa.
Pasang pengapit buaya ke grafit. Ambil satu penjepit dari klip bateri dan pasangkan pada hujung salah satu pensel. Pastikan ia menyentuh sebanyak mungkin grafit. Lakukan perkara yang sama dengan penjepit buaya dan kepingan pensil.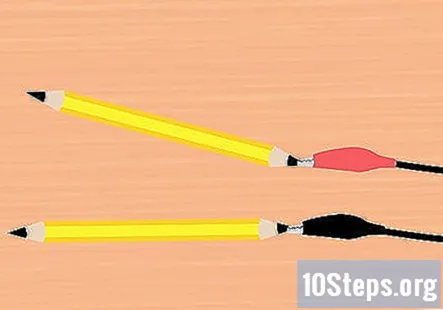
- Satu pensil harus dilekatkan pada penjepit merah dan satu pensil pada pengapit hitam.
Geser hujung pensel yang tidak ditutup ke dalam tabung uji. Pastikan tabung uji sepenuhnya terendam, condongkan sedikit sehingga anda boleh memasukkan hujung pensil yang tidak ditutup ke dalam tiub. Ulangi proses ini dengan pensil dan tabung uji yang lain.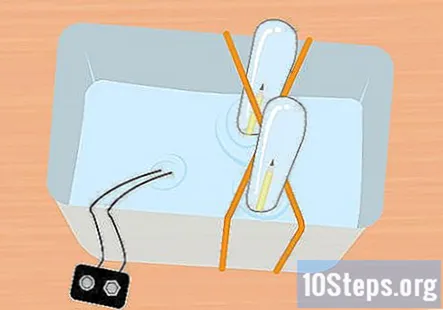
- Pada ketika ini, semuanya mesti berada di bawah air dan mesti ada satu kepingan pensil di dalam setiap tabung uji.
- Jauhkan hujung klip bateri yang melekat pada bateri dari air.
Pasang klip bateri ke bateri 9 volt. Dengan semua yang disiapkan, anda kini sudah bersedia untuk menggunakan elektrik yang disediakan oleh bateri 9 volt. Hujung klip bateri mestilah melekat keluar dari bekas sehingga cukup klip bateri di tempatnya. Setelah bateri terpasang, anda akan melihat gelembung naik dari hujung grafit dan melayang ke bahagian atas setiap tabung uji.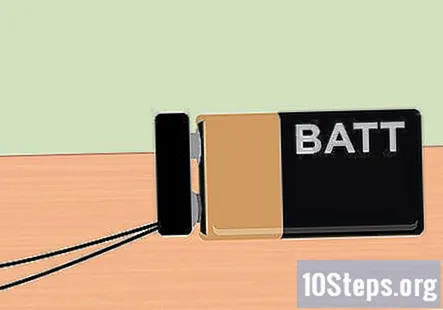
- Sekiranya anda tidak melihat gelembung dihasilkan, periksa untuk memastikan pengapit buaya terpasang dengan kuat pada grafit pensil. Juga, pastikan bateri anda sudah terisi penuh.
- Tabung uji dengan wayar negatif yang dilekatkan pada pensil akan menghasilkan hidrogen, sementara tabung uji yang dilekatkan pada wayar positif bateri akan menghasilkan oksigen.
Kumpulkan hidrogen dan oksigen dalam dua tabung uji sehingga anda mempunyai beberapa inci gas di setiap tabung. Ingat, tiub yang disambungkan ke hujung negatif bateri akan mempunyai hidrogen dan oksigen akan berada di dalam tiub yang dihubungkan ke hujung positif. Keluarkan tabung uji dari balang, satu demi satu. Terus terbalik dan biarkan air mengalir keluar. Gas di dalam tiub akan tetap ada walaupun anda tidak dapat melihatnya.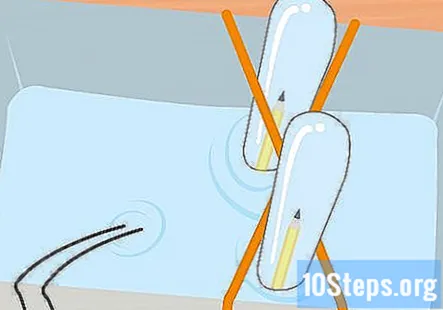
Uji keberadaan hidrogen. Anda boleh menguji keberadaan hidrogen dengan menyerang dan menyalakan api ke gas. Ia akan mengeluarkan suara "pop squeaky" yang sangat berbeza jika ia adalah hidrogen. Anda juga boleh menggunakan lilin yang menyala dan bukannya mancis.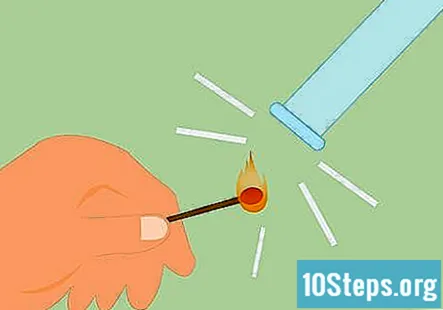
- Untuk menguji oksigen dalam tabung uji yang disambungkan ke sisi positif sumber kuasa, hembuskan padanan cahaya (atau lilin) dan letakkan hujung yang masih bersinar di bawah tabung uji. Sekiranya lilin menyala semula, oksigen ada.
Soalan dan Jawapan Komuniti
Adakah saya memerlukan dua tabung uji jika saya mahu mengumpul hidrogen sahaja?

Saintis Alam Sekitar Bess Ruff adalah pelajar PhD Geografi di Florida State University. Dia memperoleh gelar MA dalam Sains dan Pengurusan Alam Sekitar dari University of California, Santa Barbara pada tahun 2016. Dia telah menjalankan kerja tinjauan untuk projek perancangan spasial laut di Caribbean dan memberikan sokongan penyelidikan sebagai rakan siswazah untuk Kumpulan Perikanan Berkelanjutan.

Berapa banyak hidrogen yang dapat dikumpulkan dari eksperimen elektrolisis sederhana ini? Dan apakah tekanan gas hidrogen?
Itu bergantung. Kadar tindak balas (pemisahan air) didasarkan pada amp bateri dan masa yang tersisa untuk bertindak balas. Biasanya hidrogen berada pada tekanan permukaan laut kecuali anda melakukan percubaan di persekitaran yang sangat panas atau sejuk.
Mengapakah hidrogen mengumpul dalam tiub negatif
Oleh kerana molekul air berkongsi elektron, atom hidrogen dicas positif dan atom Oksigen dikenakan secara negatif. Semasa mengeluarkan gas, Hidrogen bermuatan positif akan tertarik ke tiub negatif, sementara Oksigen bercas negatif akan tertarik ke tiub positif.
Mengapa gas tidak terlepas dari tabung pengumpul gas saya?
Ia adalah hidrogen, gas yang lebih ringan daripada yang lain, termasuk helium, yang bermaksud bahawa ia akan tinggal di tabung uji selagi hujung tiub tertutup berada di atas kerana gas yang lain menggantikannya. Sebab kita menggunakan helium dan bukannya hidrogen adalah kerana ia tidak mudah terbakar. Ini disebabkan oleh fakta bahawa ia adalah gas mulia (ia mempunyai shell valensi penuh 8 elektron) dan oleh itu tidak reaktif.
Adakah gas itu sangat mudah terbakar?
Ya. Lihat bencana Hindenburg di YouTube. Zeppelins menggunakan hidrogen kerana ia adalah gas paling ringan, dan cukup mudah diperoleh. Itulah sebabnya mengapa beberapa pembuat kereta mengusahakan kereta berkuasa hidrogen.
adakah ini bentuk hidrogen cair?
Tidak - hidrogen dalam eksperimen ini akan menjadi gas
Bagaimana cara mencairkan hidrogen? Jawapan
Amaran
- Berhati-hati dengan hidrogen tulen. Ia sangat mudah meletup apabila dicampurkan dengan udara.
- Pastikan semua udara lain dikeluarkan dari peralatan tempat anda mengumpulkan hidrogen.


